Центр Валидации

Мы осуществляем валидацию процессов хранения и перевозки лекарственных средств, а также квалификацию оборудования для хранения и транспортировки термолабильной продукции, что помогает клиентам обеспечить сохранность термочувствительных грузов и гарантировать соблюдение надлежащего температурного режима, либо вовремя принять меры по устранению нарушений и слабых звеньев, допущенных в системе холодовой цепи.

Правила
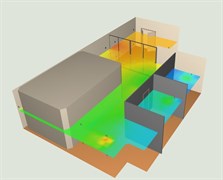
Цель картирования — официально зафиксировать существующие температурные уровни в нескольких точках определенной зоны, которая может служить для транспортировки или хранения термолабильной продукции.
Картирование складских помещений (лето, зима)
Картирование грузового автотранспорта


- IQ (installation qualification) – квалификация монтажа подтверждает, что процессили оборудование соответствует спецификациям, все компоненты и документация, необходимые для работы, присутствуют в наличии.
- OQ (operational qualification) – квалификация функционирования подтверждает, что все звенья процесса или оборудования обеспечены/организованы правильно и работают нормально.
- PQ (performance qualification) – квалификация эксплуатации подтверждает, что процесс или оборудование стабильно функционирует надлежащим образом в течение определенного времени.
- Цели, объект и объем квалификационного исследования
- Ответственность, сведения об экспертизе и составе участников квалификации
- Перечень оборудования для квалификации, условия и параметры его работы
- Выводы и заключения по итогам квалификации IQ/OQ/PQ
- Параметры калибровки для контрольного оборудования
- Критические параметры процесса и допустимые отклонения
- Схема технологического процесса
- Статистические инструменты обработки данных
- Бланки, таблицы и шаблоны для записи данных, формат отражения данных
- Выводы и результаты квалификационного исследования, утверждение отчетов
- о выполнении квалификации
- Программа/план валидации/квалификации (Validation/Qualification plan), которая включает анализ рисков, методики проведения испытаний, критерии приемлемости, перечень используемого оборудования, методики оценки.
- Протокол валидации/квалификации (Validation/Qualification protocol), который отражает ход исследования и содержит анализ проведенных испытаний и полученных данных
- Отчет по валидации/квалификации (Validation/Qualification report), который содержит выводы валидации/квалификации и предложения по проведению дальнейших мероприятий.























